La corrosion galvanique – Partie 1
La corrosion galvanique est un enjeu majeur en construction métallique, car elle peut compromettre la durabilité, la sécurité et le coût d’exploitation des ouvrages si elle n’est pas anticipée. Ce premier article va détailler le principe de la corrosion galvanique et les facteurs aggravants. Un deuxième article parlera des solutions pour éviter ce phénomène.
Qu’est-ce que la corrosion galvanique ?
Les différents métaux n’ont pas la même résistance à la corrosion. Il existe une échelle de potentiel électrochimique (échelle galvanique) qui classe ces métaux du moins « noble » au plus « noble ».
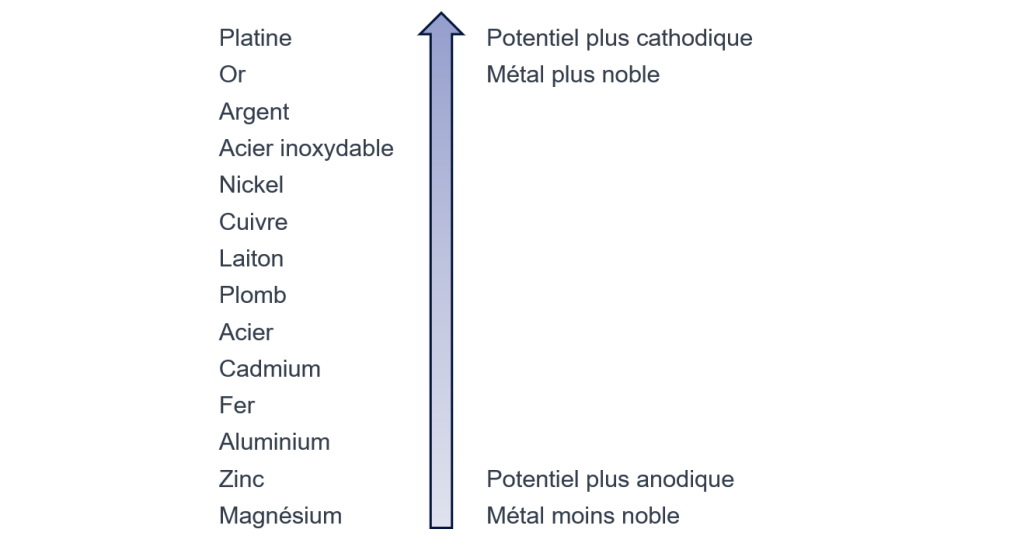
La corrosion galvanique est un phénomène électrochimique qui se produit lorsque deux métaux différents sont en contact électrique en présence d’un électrolyte (eau, eau salée, béton humide…). Le métal le moins « noble » (anode) cède des électrons et se corrode, tandis que le métal le plus « noble » (cathode) capte les électrons et n’est pas attaqué. Le mouvement des électrons résulte d’une différence de potentiel entre les métaux, exprimée par la série galvanique. Ce processus est accéléré si l’échange d’ions dans l’électrolyte est facile (forte conductivité, présence de chlorures, humidité élevée…).
Facteurs influençant la corrosion galvanique
Plusieurs facteurs vont exercer une influence plus ou moins importante sur la réaction de corrosion.
La différence de potentiel entre métaux est le paramètre le plus impactant : plus l’écart est grand dans la série galvanique, plus le risque est élevé. On admet qu’il faille une différence d’environ 300 millivolts (mV) entre les deux métaux pour que ce phénomène de corrosion galvanique soit significatif, exemples :
- Aluminium / Acier inoxydable : » 900 mV ; corrosion de l’aluminium,
- Zinc / Acier inoxydable : » 900 mV ; corrosion du zinc,
- Zinc / Acier : » 400 mV ; corrosion du zinc,
- Zinc / Cuivre : » 850 mV ; corrosion du zinc,
- Acier / Cuivre : » 450 mV ; corrosion de l’acier.
Le rapport de surfaces entre la cathode et l’anode est également un paramètre important : une petite surface anodique face à une grande cathode entraînera une densité de courant élevée sur l’anode et une corrosion rapide. Inversement une petite surface cathodique aura normalement peu d’influence sur une grande surface anodique selon l’environnement. (voir en complément l’article du 6 juin 2022 « Résistance à la corrosion des fixations »)
La présence d’un électrolyte est essentielle pour avoir une corrosion galvanique mais la nature de celui-ci peut influencer l’intensité du phénomène : une atmosphère marine, une eau salée, ou une eau chargée en ions (chlorures, sulfates…) ayant une conductivité plus élevée qu’une eau douce par exemple augmentera le phénomène de corrosion.
La conception mécanique (zones de rétention d’eau et de polluants, interstices et espacements étroits, point de contact par boulonnerie…) emplifiera la corrosion.
La qualité, continuité et l’état (rayures, défauts) des revêtements et passivation déterminent la protection.
La température et le pH : la corrosion augmente souvent avec la température et en présence de pH extrême.
Les courants vagabonds ou courants de fuite sont également des sources externes de courant qui peuvent aggraver la corrosion.
Exemples concrets et assemblages problématiques fréquents
- Fixations en acier galvanisé sur une structure en acier inoxydable extérieure → le zinc de la galvanisation puis l’acier (moins nobles) vont se corroder
- Aluminium en contact avec acier inoxydable en milieu marin → l’aluminium (métal moins noble) se corrode rapidement.
- Acier galvanisé en contact avec cuivre/bronze → le zinc sert d’anode sacrificielle, mais si la couche est compromise, l’acier peut être attaqué.
- Fixations en acier inox sur profils en aluminium ou acier ordinaire en zones salines → corrosion locale autour des fixations.
Références
RODIER A., Résistance à la corrosion des fixations, Métalétech, juin 2022.
Olivier Mouatt, directeur de projets matériaux et corrosion, CTICM